超大基因组研究集锦——动物篇
“Why are some genomes so big and others very small?”这是Science杂志发布的125个前沿科学问题之一。物种的基因组大小不尽相同,造成这一现象的原因十分复杂。研究表明,基因组大小的差异不仅与生物体的复杂性有关,还与其生活史特征、环境适应性、基因家族的扩增和基因重组等因素密切相关,如此复杂重要的问题吸引了无数研究者深入探索这一领域。
相较于易于研究的小型基因组生物,具有超大型基因组的生物种类繁多、保守的遗传变异丰富,这为比较基因组学研究提供了极好的材料。然而,由于超大基因组中高重复序列的存在以及广阔的基因间区,传统二代测序技术难以为这些生物构建Gap-free级别的的参考基因组。
近年,单分子实时测序等三代长读长技术的出现为超大基因组组装提供了转机。三代测序以其长读长的优势(ONT Ultra-long测序技术N50可达100-150Kb),破解了重复区组装中的难题,使得研究人员能够通过三代数据进行染色体水平的整体组装。此外,三代测序超长读长的reads能够贯穿基因组中的基因间区。这使得非编码RNA、调控元件以及结构变异都能被准确检测。因此,通过单分子实时测序技术,研究人员能够更好地探究超大基因组的复杂性和结构,揭示其中的重复序列、基因间区和功能元件。这为研究人员深入理解基因组大小差异的形成机制、进化过程以及生物体的适应性提供了重要的工具和方法。
希望组着眼于三代测序技术应用于超大基因组研究中所带来的革新与价值,为有志于研究超大基因组物种的研究人员提供专业的测序、组装、分析服务。希望组以其优质的测序服务质量和遥遥领先的基因组组装技术受到了各位专家老师的认可,非常荣幸能够参与多个超大基因组的研究之中,为生命科学领域做出了独属于希望组的贡献。
下面是希望组合作的几篇超大基因组动物篇的优秀文章:
01. The enormous repetitive Antarctic krill genome reveals environmental adaptations and population insights
目标物种:南极磷虾(Antarctic krill)
发表时间:2023.05
发表期刊:Cell(IF=64.5)
合作单位:中国水产科学研究院黄海水产研究所、德国阿尔弗雷德·魏格纳研究所、澳大利亚联邦科学与工业研究组织
测序策略:PacBio HiFi、Illumina、Hi-C
基因组大小:48.01 Gb
基因组Contig N50:178.99Kb
该研究完成了迄今为止最大动物基因组参考序列——南极磷虾基因组组装,并揭示了南极磷虾适应极端环境和群体历史演化的分子基础。研究者利用PacBio、Hi-C结合短读长对南极磷虾进行测序,使用NextDenovo v2.30 组装了48.01Gb的基因组。研究发现,南极磷虾重复序列含量高达92.45%,这源于南极磷虾基因组重复序列的两次爆发式扩张。在该研究中,研究人员对其抗饿和对极昼极夜环境的适应性进行了研究。结果发现,在磷虾基因组里鉴定得到的25个显著扩张的基因家族中,分别有6个基因家族与磷虾蜕壳及能量代谢相关。这表明,蜕壳和能量代谢相关基因的改变是南极磷虾对南大洋不稳定食物供应的适应。另外,研究团队还发现,虽然分布在不同的区域,但南极磷虾的遗传序列组成没有明显区别,这就意味着不同地域群体之间没有实质性差异,并且气候变化影响着南极磷虾种群的规模。武汉希望组为本研究提供基因组组装服务,武汉希望组首席生信技术官胡江为共同作者。

论文链接:https://doi.org/10.1016/j.cell.2023.02.005
02. African lungfish genome sheds light on the vertebrate water-to-land transition
目标物种:非洲肺鱼(African lungfish)
发表时间:2021.03
发表期刊:Cell(IF=64.5)
合作单位:西北工业大学生态与环境学院、中国科学院水生生物研究所淡水生态与生物技术国家重点实验室、中国科学院昆明动物研究所遗传资源与进化国家重点实验室
测序策略:Nanopore Ultra-long、BioNano、Hi-C
基因组大小:40.05 Gb
基因组Contig N50:1.60 Mb
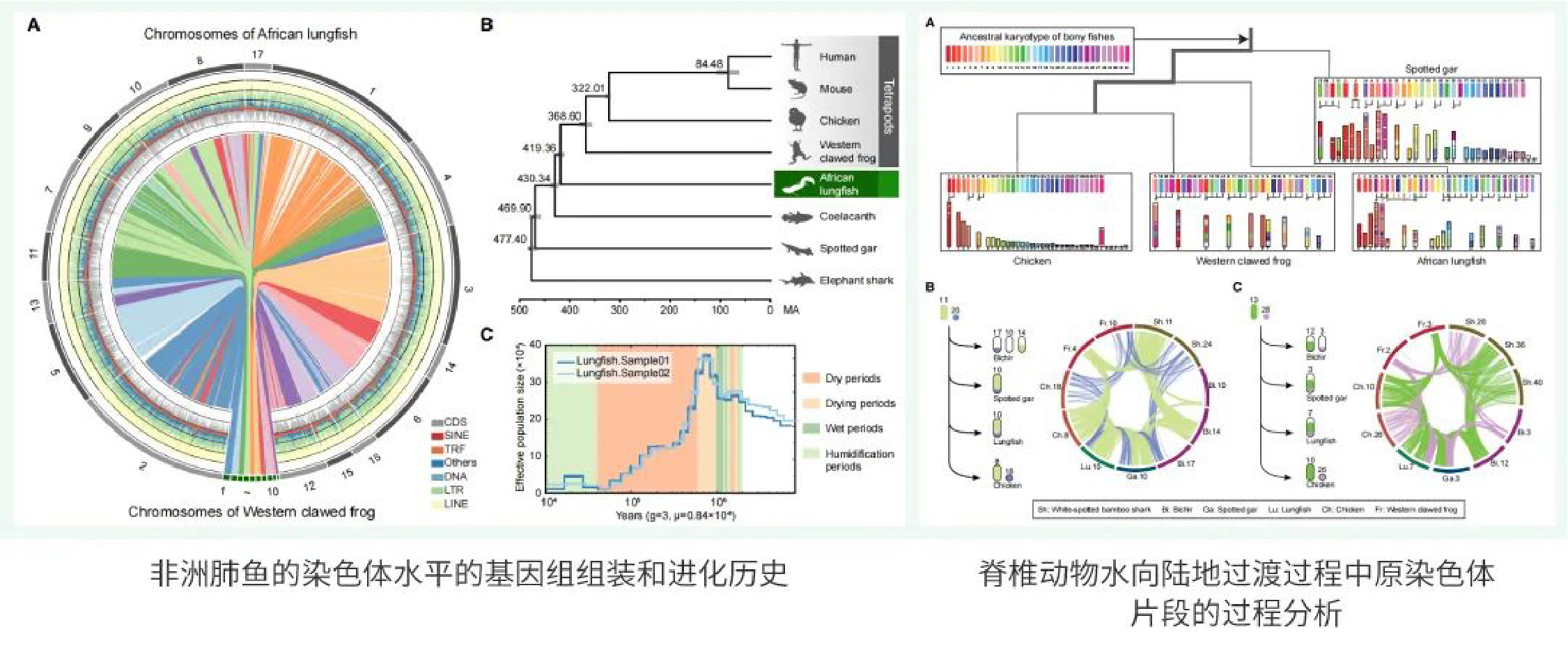
研究团队利用Nanopore Ultra-long、BioNano和Hi-C测序,采用NextDenovo + wtdbg2 + NextPolish策略组装,最终获得约40.05 Gb的基因组,Contig N50达到1.60 Mb;结合BioNano和Hi-C数据对基因组构建Scaffold和辅助染色体挂载,最终得到17条染色体,Scaffold N50 2.81 Gb,染色体挂载率达到99%以上。BUSCO评估显示该基因组包含了95%以上的脊椎动物完整基因。非洲肺鱼基因组如此巨大主要是由TEs的扩张引起的,非洲肺鱼基因组的61.7%(24.7 Gb)被注释为重复序列。研究团队通过分析Kimura distance估算了TE历史扩张活动,结果表明TEs,特别是反转录转座子,在过去7000万年中一直活跃。基于基因组组装和注释结果,通过对8种脊椎动物的5149个单拷贝基因进行系统发育重建,证实非洲肺鱼是与四足动物最近的姐妹谱系,非洲肺鱼和四足动物的分化时间可追溯到泥盆纪伊始,估算为419 MA。希望组为研究提供基因组测序和NextDenovo、NextPolish软件及组装技术支持,希望组首席生信技术官胡江参与本研究。
论文链接:https://doi.org/10.1016/j.cell.2021.01.047
03. Giant lungfish genome elucidates the conquest of land by vertebrates
目标物种:澳洲肺鱼(Giant lungfish)
发表时间:2021.01
发表期刊:Nature (IF=64.8)
合作单位:德国康斯坦茨大学生物系、德国维尔茨堡大学生物中心
测序策略:Nanopore 1D 、Ultra-long、Hi-C
基因组大小:37 Gb
基因组Contig N50:1.86Mb
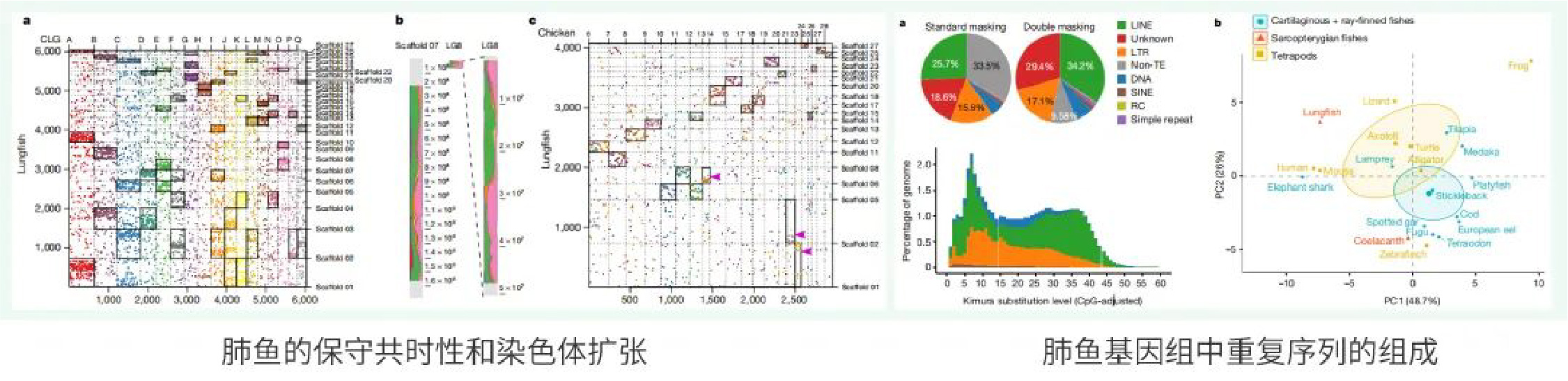
研究者利用Nanopore 1D 和Ultra-long技术对澳洲肺鱼进行了全基因组测序组装,最终组装出37Gb,Contig N50达1.86Mb的澳洲肺鱼基因组。之后利用271Gb Hi-C 数据,对基因组进行染色体级别组装,最终得到Scaffold N50 1.75Gb,组装出了17条大染色体和10条小染色体。BUSCO评估组装的基因组包含67%的脊椎动物完整基因。肺鱼是属于肉鳍鱼类中的一类,肉鳍鱼的叶状鳍在进化中最终形成了适于陆地爬行的足趾。通过比较基因组分析,研究者对保守的四足动物肢体增强元件的分析表明,有31种起源于肉鳍类。与sall1相关的hs72增强子驱动掌部区域基因表达。sall1在肺鱼胚胎中高表达,并呈现类似于四足动物的表达模式,但在斑马鱼的鳍发育过程中不表达。这表明该基因功能和肺鱼的肉鳍类叶状鳍发育相关。hoxc基因在双鳍和四肢中的表达仅在与甲床相关的哺乳动物中报道过,而RNA-seq分析发现在肺鱼幼体鳍部hoxc基因有表达。研究者还发现hoxc13在蝾螈肢中表达,在辐鳍鱼的胸鳍中不表达,转录本定位显示hoxc13也在肺鱼胚胎远端鳍表达。这表明在四足动物中,该基因结构域可能调控肢体元素生成,如指甲、蹄和爪。hoxc与sall1一起,证明了早期肉鳍类起源的四肢样基因表达促进了鳍肢过渡。希望组为本研究提供Nanopore Ultra-long测序服务。
论文链接:https://doi.org/10.1038/s41586-021-03198-8





发表评论
想参加讨论吗?请尽情讨论吧!